Is LiTFSI de beste keuze om de prestaties bij lage temperaturen in HEV-cellen te verbeteren?
| Jerry Huang
Over het algemeen wordt aangenomen dat hoe hoger het aandeel harde koolstof (meer dan 15%) op de anode van een li-ionbatterij is gecoat, hoe beter de geleidbaarheid ervan. We moeten echter duidelijk maken dat de verdichting van hengelstukken van puur hard carbon ongeveer 1,15 g/cc is. Als er meer harde koolstof op het grafietmateriaal wordt gecoat, wordt de verdichtingsdichtheid van het gehele poolstuk verminderd (zonder de ruimte tussen de kernmateriaallagen te vergroten). Het kan maximaal 1,2 g/cc bereiken. Tegelijkertijd kan de harde koolstof worden verdicht en wordt de prestatie mogelijk niet volledig benut. Daarom is het noodzakelijk om verschillende verhoudingen van harde koolstofcoating te kiezen op basis van toepassingsscenario's.
Het is logisch dat het anodemateriaal gewoonlijk ongelijk gespannen en onregelmatig is. Hoe groter de deeltjesgrootte van het materiaal, hoe groter de interne weerstand. Daarom, als een harde koolstofcoating wordt gebruikt, hoewel de levensduur van de batterij aanzienlijk kan worden verlengd, is de levensduur van de batterij relatief slecht (de capaciteit van de batterijcel neemt sterk af bij opslag van 6 maanden).
Is LiTFSI de beste keuze om de prestaties bij lage temperaturen in HEV-cellen te verbeteren?
Het is duidelijk dat hard met koolstof gecoat anodemateriaal niet voldoende is om de pijnpunten van slechte prestaties bij lage temperaturen op te lossen; sommige andere materialen moeten worden verbeterd, zoals elektrolyten. Elektrolyten vormen een belangrijk onderdeel van lithium-ionbatterijen en ze bepalen niet alleen de migratiesnelheid van Li+ lithiumionen in de vloeibare fase, maar spelen ook een sleutelrol bij de vorming van SEI-film. Tegelijkertijd hebben de bestaande elektrolyten een lagere diëlektrische constante, zodat lithiumionen meer oplosmiddelmoleculen kunnen aantrekken en deze kunnen vrijgeven tijdens desolvatie, wat leidt tot grotere systeementropieveranderingen en hogere temperatuurcoëfficiënten (TC's). Daarom is het belangrijk om een modificatiemethode te vinden die een kleinere entropieverandering heeft tijdens desolvatie, een lagere temperatuurcoëfficiënt en minder wordt beïnvloed door de elektrolytconcentratie. Momenteel zijn er twee manieren om de prestaties bij lage temperaturen te verbeteren door middel van elektrolyten:
- Verbeter de geleidbaarheid van elektrolyten bij lage temperaturen door de samenstelling van het oplosmiddel te optimaliseren. De prestatie van elektrolyten bij lage temperaturen wordt bepaald door het eutectische punt bij lage temperatuur. Als het smeltpunt te hoog is, zal het elektrolyt waarschijnlijk uitkristalliseren bij lage temperaturen, wat de geleidbaarheid van elektrolyten ernstig zal beïnvloeden en uiteindelijk zal leiden tot uitval van de lithiumbatterij. EC-ethyleencarbonaat is een belangrijk oplosmiddelbestanddeel van de elektrolyt. Het smeltpunt is 36°C. Bij lage temperaturen zal de oplosbaarheid waarschijnlijk afnemen en zelfs kristallen worden neergeslagen in elektrolyten. Door toevoeging van laagsmeltende en laagviskeuze componenten om het EC-gehalte van het oplosmiddel te verdunnen en te verlagen, kunnen de viscositeit en het eutectische punt van de elektrolyt bij lage temperaturen effectief worden verlaagd en kan de geleidbaarheid van elektrolyten worden verbeterd. Bovendien hebben binnenlandse en buitenlandse studies ook aangetoond dat het gebruik van ketencarbonzuur, ethylacetaat, ethylpropionaat, methylacetaat en methylbutyraat als het elektrolyt-co-oplosmiddel gunstig is voor de verbetering van de geleidbaarheid bij lage temperaturen van elektrolyten en verbetert de prestaties van de batterij bij lage temperaturen aanzienlijk. Op dit gebied is aanzienlijke vooruitgang geboekt.
- Het gebruik van nieuwe additieven om de eigenschappen van de SEI-film te verbeteren, maakt het bevorderlijk voor de geleiding van lithiumionen bij lage temperaturen. Elektrolytzout is een van de belangrijke componenten van elektrolyten en het is ook een sleutelfactor om uitstekende prestaties bij lage temperaturen te verkrijgen. Het elektrolytzout dat sinds 2021 op grote schaal wordt gebruikt, is lithiumhexafluorfosfaat. De SEI-film die gemakkelijk wordt gevormd na veroudering, heeft een grote impedantie, wat resulteert in slechte prestaties bij lage temperaturen. Daarom wordt de ontwikkeling van een nieuw type lithiumzout urgent. Lithiumtetrafluorboraat en lithiumdifluoroxalaatboraat (LiODFB), als lithiumzouten voor elektrolyt, hebben ook geleid tot een hoge geleidbaarheid bij hoge en lage temperaturen, zodat de lithiumionbatterij uitstekende elektrochemische prestaties vertoont in een breed temperatuurbereik.
Als een nieuw type niet-waterig lithiumzout heeft LiTFSI een hoge thermische stabiliteit, een kleine mate van associatie van anion en kation, en een hoge oplosbaarheid en dissociatie in carbonaatsystemen. Bij lage temperaturen zorgen de hoge geleidbaarheid en lage ladingsoverdrachtsweerstand van het LiFSI-systeemelektrolyt voor zijn prestaties bij lage temperaturen. Mandal et al. heeft LiTFSI gebruikt als lithiumzout en EC/DMC/EMC/pC (massaverhouding 15:37:38:10) als het basisoplosmiddel voor elektrolyt; en het resultaat toonde aan dat de elektrolyt nog steeds een hoge geleidbaarheid heeft van 2 mScm-1 bij -40°C. Daarom wordt LiTFSI beschouwd als de meest veelbelovende elektrolyt die lithiumhexafluorfosfaat kan vervangen, en wordt ook beschouwd als een alternatief voor de overgang naar een tijdperk van vaste elektrolyten.
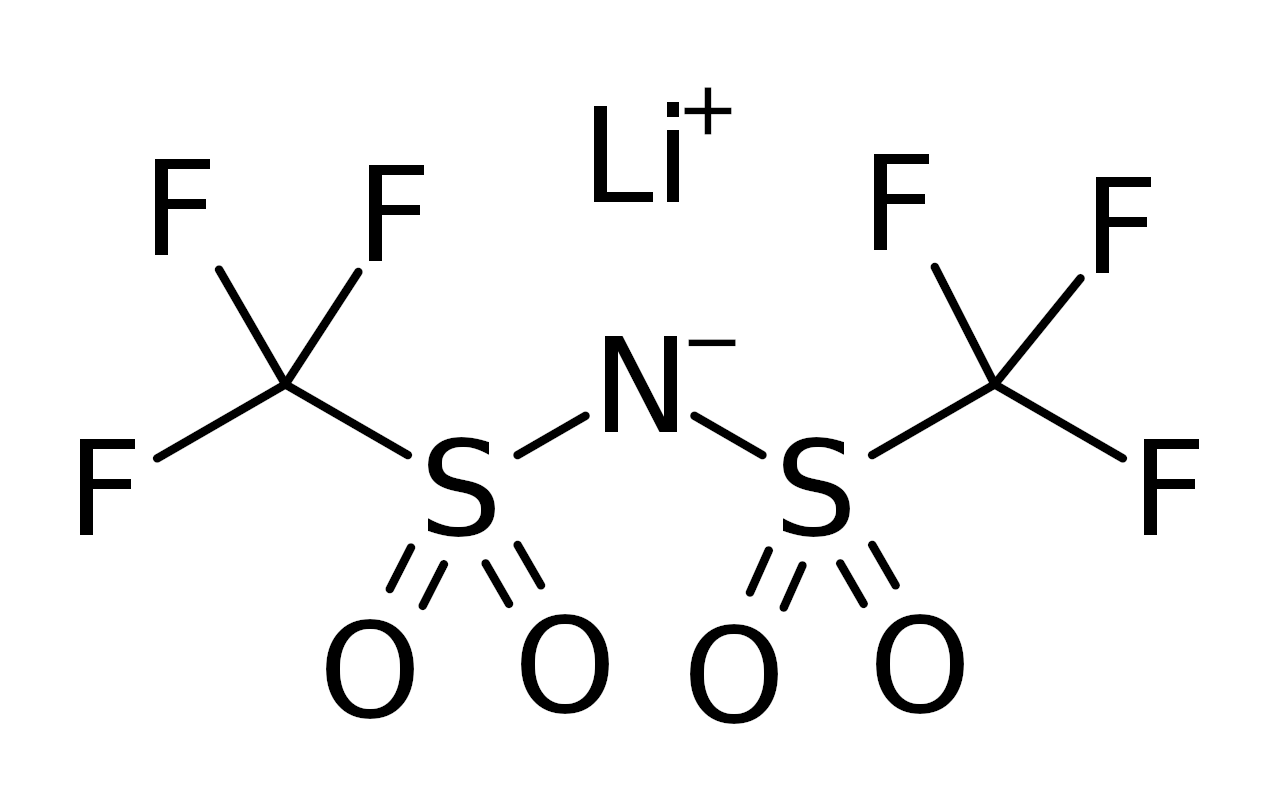
Volgens Wikipedia is Lithium bis(trifluormethaansulfonyl)imide, vaak eenvoudigweg LiTFSI genoemd, een hydrofiel zout met de chemische formule LiC2F6NO4S2. LiTFSI is een wit kristal of poeder dat kan worden gebruikt als een organisch elektrolyt-lithiumzout voor lithium-ionbatterijen, waardoor het elektrolyt een hoge elektrochemische stabiliteit en geleidbaarheid vertoont. Het wordt vaak gebruikt als Li-ionbron in elektrolyten voor Li-ionbatterijen als een veiliger alternatief voor het veelgebruikte lithiumhexafluorfosfaat. Het bestaat uit één Li-kation en een bistriflimide-anion. Vanwege de zeer hoge oplosbaarheid in water (> 21 m) is LiTFSI gebruikt als lithiumzout in water-in-zoutelektrolyten voor waterige lithium-ionbatterijen.
LiTFSI kan worden verkregen door de reactie van bis(trifluormethylsulfonyl)imide en lithiumhydroxide of lithiumcarbonaat in een waterige oplossing, en het watervrije kan worden verkregen door vacuümdrogen bij 110 °C: LiOH + HNTf2 → LiNTf2 + H2O
Lithiumbis(trifluormethylsulfonyl)imide kan worden gebruikt om elektrolyten voor lithiumbatterijen te bereiden en als een nieuwe Lewis-zuurkatalysator in zeldzame aarde; het wordt gebruikt om chirale imidazoliumzouten te bereiden door anionvervangingsreactie van overeenkomstige trifluormethaansulfonaten. Dit product is een belangrijke fluorhoudende organische ionenverbinding, die wordt gebruikt in secundaire lithiumbatterijen, supercondensator Chemicalbook, aluminium elektrolytische condensatoren, hoogwaardige niet-waterige elektrolytmaterialen en als nieuwe hoogrenderende katalysator. Het basisgebruik is als volgt:
- Lithium batterijen
- Ionische vloeistoffen
- antistatisch
- Geneeskunde (veel minder vaak voor)
Een R&D-ingenieur uit China zei ooit: "LiTFSI wordt voornamelijk gebruikt als additief in huidige elektrolyten en zal niet alleen als het belangrijkste zout worden gebruikt. Bovendien, zelfs als het als additief wordt gebruikt, heeft de geformuleerde elektrolyt betere prestaties dan andere elektrolyten. LiTFSI-elektrolyt is veel duurder dan de gebruikelijke soorten elektrolyten, dus LiTFSI wordt niet toegevoegd als er geen speciale vereisten zijn voor de elektrolytprestaties."
Er wordt aangenomen dat er in sommige toepassingsscenario's substantiële vereisten zijn voor batterijen met hoog vermogen, scenario's zoals elektrische vorkheftrucks en AGV's. Wat betreft duurzaamheid en eigenschappen van productiegereedschappen, is het ook noodzakelijk om de problemen van de levensduur en prestaties bij lage temperaturen in één keer op te lossen. Daarom zullen onderzoek en ontwikkeling op het gebied van elektrolyten van de volgende generatie worden voortgezet. Maar het is nog steeds een multidimensionale zorg en concurrentie van prestaties, kosten en veiligheid; en de markten zullen uiteindelijk hun eigen keuzes maken.
Referenties:
- Zheng, Honghe; Qu, Qunting; Zhang, Li; Liu, Gao; Battaglia, Vincent (2012). "Harde koolstof: een veelbelovende lithium-ion batterij anode voor toepassingen bij hoge temperaturen met ionische elektrolyt". RSC gaat vooruit. Royal Society of Chemistry. (11): 4904-4912. doi:10.1039/C2RA20536J. Ontvangen 2020-08-15.
- Kamiyama, Azusa; Kubota, Kei; Nakano, Takeshi; Fujimura, Shun; Shiraishi, Soshi; Tsukada, Hidehiko; Komaba, Shinichi (27-01-2020). "Hoge capaciteit harde koolstof gesynthetiseerd uit macroporeuze fenolhars voor natrium-ion- en kalium-ionbatterij". ACS toegepaste energiematerialen. Amerikaanse Chemische Vereniging. 3: 135-140. doi:10.1021/acsaem.9b01972.
- Khosravi, Mohsen; Bashirpour, Neda; Nematpour, Fatemeh (2013-11-01). "Synthese van harde koolstof als anodemateriaal voor lithium-ionbatterijen". Geavanceerd materiaalonderzoek. 829: 922-926. doi:10.4028/www.scientific.net/AMR.829.922. S2CID 95359308. Opgehaald op 15-08-2020.
- Goriparti, Subrahmanyam; Miele, Ermanno; De Angelis, Francesco; Di Fabrizio, Enzo; Proietti Zaccaria, Remo; Capiglia, Claudio (2014). "Review over de recente voortgang van nanogestructureerde anodematerialen voor Li-ionbatterijen". Tijdschrift van krachtbronnen. 257: 421-443. Bibcode:2014JPS...257..421G. doi:10.1016/j.jpowsour.2013.11.103.
- Irisarri, E; Ponrouch, A; Palacin, MR (2015). "Review-Hard Carbon Negative Electrode Materials voor natrium-ionbatterijen". Tijdschrift van de Electrochemical Society. 162: A2476. doi:10.1149/2.0091514jes.
- Dou, Xinwei; Hasa, Ivana; Saurel, Damien; Vaalma, Christoph; Wu, kalk; Buchholz, Daniël; Bresser, Dominicus; Komaba, Shinichi; Passerini, Stefano (2019). "Harde koolstoffen voor natrium-ionbatterijen: Structuur, analyse, duurzaamheid en elektrochemie". Materialen vandaag. 23: 87-104. doi:10.1016/j.mattod.2018.12.040