Wat is Lithiumhydroxide en waar gaan we gebruiken?
| Jerry Huang
Lithiumhydroxide is een sterke base en de chemische eigenschappen lijken meer op de Groep 2-hydroxiden in het periodiek systeem, in plaats van de Groep 1-hydroxiden. Lithiumhydroxide, chemische formule als LiOH, molecuulgewicht 23,95, wit tetragonaal kristal, is intens corrosief en irriterend voor de menselijke huid, met een smeltpunt van 450 ℃ (842 ℉), relatieve dichtheid als 1,46. De differentiatietemperatuur is 924℃ (1695℉). Het is enigszins oplosbaar in ethanol, oplosbaar in water, maar de oplosbaarheid is lager dan die van hydroxiden van andere alkalimetalen.
Na absorptie van vocht in de lucht of kristallisatie in een waterige oplossing wordt het lithiumhydroxide-monohydraat verkregen. Lithiumhydroxide reageert met zure gassen zoals zwaveldioxide, waterstofchloride, waterstofcyanide, enz. Het kan ook volledig reageren met sterke of zwakke zuren in waterige oplossingen. Het absorbeert koolstofdioxide in de lucht om lithiumcarbonaat te produceren. Lithiumhydroxide wordt gebruikt als vetadditief (verdikkingsmiddel, antioxidant, middel voor extreme druk), dat de hittebestendigheid, waterbestendigheid, stabiliteit en mechanische eigenschappen kan verbeteren; en vet op lithiumbasis wordt vaak gebruikt voor lagers in auto's, treinen, vliegtuigen, kranen en alle kostbare machines.
Lithiumhydroxide-batterijkwaliteit, met een laag smeltpunt, is algemeen aanvaard als een beter elektrolytmateriaal bij de NCA, NCM-lithium-ionbatterijproductie, waardoor nikkelrijke lithiumbatterijen veel betere elektrische eigenschappen hebben dan lithiumcarbonaat; terwijl de laatste tot nu toe de prioriteit blijft voor LFP en vele andere batterijen.
Het geroosterde vaste lithiumhydroxide kan worden gebruikt als koolstofdioxide-absorberend middel voor bemanningen in ruimtevaartuigen en onderzeeërs. Kooldioxide kan gemakkelijk worden opgenomen in gas dat waterdamp bevat. De chemische reactieformule is als volgt: 2LiOH+CO2→Li2CO3+H2O
Eén gram watervrij lithiumhydroxide kan 450 ml koolstofdioxide opnemen en 750 g is voldoende om alle uitgeademde koolstofdioxide van één persoon op een hele dag te absorberen. Daarnaast wordt lithiumhydroxide voornamelijk gebruikt om verschillende lithiumverbindingen en lithiumzouten te produceren, evenals lithiumzepen, op lithium gebaseerde vetten en alkydharsen. En het wordt veel gebruikt als katalysatoren, fotografische ontwikkelaars, ontwikkelmiddelen voor spectrale analyse, additieven in alkalinebatterijen. Als additief voor alkalinebatterij-elektrolyt kan lithiumhydroxide de elektrische capaciteit met 12% tot 15% en de levensduur van de batterij met 2 of 3 keer verhogen.
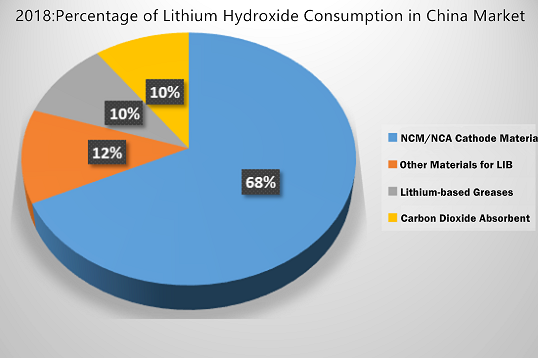
Hier is een foto van het verbruik van lithiumhydroxide op de Chinese markt in 2018, ter referentie.