| Jerry Huang
ข่าวจากงานแสดงสินค้าอิเล็กทรอนิกส์สำหรับผู้บริโภค (CES) 2026 ที่ลาสเวกัส บริษัทสตาร์ทอัพสัญชาติฟินแลนด์ Donut Lab ได้นำเสนอผลิตภัณฑ์ "เทคโนโลยีสีดำ" ที่ล้ำสมัยของพวกเขาในงาน CES ประจำปี โดยบริษัทนี้อ้างว่าแบตเตอรี่ของตนเป็นแบตเตอรี่โซลิดสเตททั้งหมด (ASSB) ที่ผลิตในปริมาณมากเป็นครั้งแรกของโลก ในงาน CES 2026 Donut Lab ได้ประกาศเปิดตัวสิ่งที่พวกเขาเรียกว่าแบตเตอรี่โซลิดสเตทแบบเต็มรูปแบบรุ่นแรกของโลก ซึ่งพร้อมสำหรับการผลิตในระดับ OEM และจะเป็นแบตเตอรี่ชนิดแรกที่จะนำไปใช้กับรถจักรยานยนต์รุ่น TS Pro และ Ultra ของ Verge Motorcycles หากสามารถส่งมอบให้กับลูกค้าได้จริง นี่จะเป็นก้าวสำคัญในเส้นทางการใช้พลังงานไฟฟ้าทั่วโลก โดยเป็นการบ่งชี้ถึงการเปลี่ยนผ่านของเทคโนโลยีโซลิดสเตทจากห้องปฏิบัติการไปสู่การผลิตจำนวนมาก
ในงาน CES 2026 Donut Lab ได้ประกาศเปิดตัวสิ่งที่พวกเขาเรียกว่าแบตเตอรี่โซลิดสเตทแบบเต็มรูปแบบรุ่นแรกของโลก ซึ่งพร้อมสำหรับการผลิตในระดับ OEM และจะเป็นแบตเตอรี่ชนิดแรกที่จะนำไปใช้กับรถจักรยานยนต์รุ่น TS Pro และ Ultra ของ Verge Motorcycles หากสามารถส่งมอบให้กับลูกค้าได้จริง นี่จะเป็นก้าวสำคัญในเส้นทางการใช้พลังงานไฟฟ้าทั่วโลก โดยเป็นการบ่งชี้ถึงการเปลี่ยนผ่านของเทคโนโลยีโซลิดสเตทจากห้องปฏิบัติการไปสู่การผลิตจำนวนมาก ในข่าวประชาสัมพันธ์บนเว็บไซต์อย่างเป็นทางการ Donut Lab ระบุว่า บริษัทมุ่งมั่นที่จะคิดค้นและนำเสนอโซลูชันด้านการใช้พลังงานไฟฟ้าแบบใหม่ๆ โดยผลักดันขีดจำกัดด้านประสิทธิภาพของยานยนต์ไฟฟ้าอย่างไม่หยุดยั้ง และนำเทคโนโลยีใหม่ๆ สู่ตลาด Donut Lab กำลังกำหนดอนาคตของการคมนาคมขนส่ง “ขณะนี้ Donut Lab รู้สึกเป็นเกียรติอย่างยิ่งที่ได้เปิดตัวแบตเตอรี่โซลิดสเตทตัวแรกของโลกที่สามารถนำไปใช้ในการผลิตยานยนต์ OEM ได้ แบตเตอรี่โซลิดสเตทของ Donut Lab จะถูกนำไปใช้งานเชิงพาณิชย์ทันที เพื่อให้พลังงานแก่รถจักรยานยนต์ Verge รุ่นปัจจุบัน”
ในข่าวประชาสัมพันธ์บนเว็บไซต์อย่างเป็นทางการ Donut Lab ระบุว่า บริษัทมุ่งมั่นที่จะคิดค้นและนำเสนอโซลูชันด้านการใช้พลังงานไฟฟ้าแบบใหม่ๆ โดยผลักดันขีดจำกัดด้านประสิทธิภาพของยานยนต์ไฟฟ้าอย่างไม่หยุดยั้ง และนำเทคโนโลยีใหม่ๆ สู่ตลาด Donut Lab กำลังกำหนดอนาคตของการคมนาคมขนส่ง “ขณะนี้ Donut Lab รู้สึกเป็นเกียรติอย่างยิ่งที่ได้เปิดตัวแบตเตอรี่โซลิดสเตทตัวแรกของโลกที่สามารถนำไปใช้ในการผลิตยานยนต์ OEM ได้ แบตเตอรี่โซลิดสเตทของ Donut Lab จะถูกนำไปใช้งานเชิงพาณิชย์ทันที เพื่อให้พลังงานแก่รถจักรยานยนต์ Verge รุ่นปัจจุบัน”
จากรายงานระบุว่า แบตเตอรี่แบบโซลิดสเตททั้งหมดของ Donut Lab มีความหนาแน่นพลังงาน 400 Wh/kg ทำให้สามารถวิ่งได้ไกลขึ้น โครงสร้างเบาลง และมีความยืดหยุ่นอย่างที่ไม่เคยมีมาก่อนในการออกแบบยานยนต์และผลิตภัณฑ์
แบตเตอรี่สามารถชาร์จจนเต็มได้ในเวลาเพียง 5 นาที โดยไม่จำเป็นต้องจำกัดการชาร์จไว้ที่ 80% และรองรับการคายประจุจนหมดอย่างปลอดภัย ซ้ำได้ และเชื่อถือได้
แตกต่างจากแบตเตอรี่ลิเธียมไอออนแบบดั้งเดิม แบตเตอรี่แบบโซลิดสเตทนี้มี “การลดลงของความจุเพียงเล็กน้อย” ตลอดอายุการใช้งาน มีการอ้างว่าผ่านการทดสอบแล้วว่าสามารถชาร์จได้ถึง 100,000 รอบ ซึ่งให้อายุการใช้งานที่ยาวนานกว่าเทคโนโลยีที่มีอยู่เดิมมาก ความปลอดภัยเป็นอีกคุณสมบัติหลักของแบตเตอรี่นี้: ไม่มีอิเล็กโทรไลต์เหลวที่ติดไฟได้ ไม่มีปฏิกิริยาความร้อนสูงเกินไป และไม่มีเดนไดรต์โลหะ! สิ่งนี้ช่วยขจัดสาเหตุของการเกิดไฟไหม้แบตเตอรี่ได้อย่างสิ้นเชิง ทำให้มีความปลอดภัยสูงและเป็นการปฏิวัติวงการอย่างแท้จริง 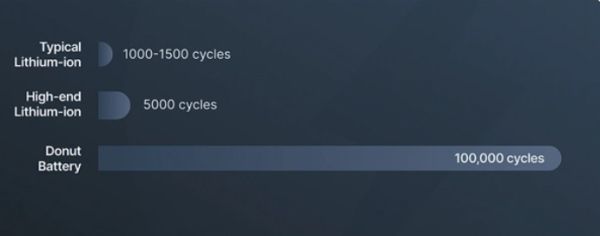 Donut Lab ระบุว่าประสิทธิภาพของแบตเตอรี่ได้รับการทดสอบอย่างเข้มงวดในอุณหภูมิที่ตั้งแต่ -30 ถึงมากกว่า 100 องศาเซลเซียส (โดยยังคงรักษาความจุได้ 99 เปอร์เซ็นต์ “โดยไม่มีสัญญาณของการติดไฟหรือการเสื่อมสภาพ”)
Donut Lab ระบุว่าประสิทธิภาพของแบตเตอรี่ได้รับการทดสอบอย่างเข้มงวดในอุณหภูมิที่ตั้งแต่ -30 ถึงมากกว่า 100 องศาเซลเซียส (โดยยังคงรักษาความจุได้ 99 เปอร์เซ็นต์ “โดยไม่มีสัญญาณของการติดไฟหรือการเสื่อมสภาพ”)
ในแง่ของวัตถุดิบและต้นทุน Donut Lab ระบุว่าแบตเตอรี่โซลิดสเตทของตนผลิตจาก “วัสดุที่หาได้ง่าย ราคาไม่แพง และปลอดภัยในเชิงภูมิรัฐศาสตร์” โดยปราศจากธาตุหายาก และมีต้นทุนต่ำกว่าแบตเตอรี่ลิเธียมไอออน อย่างไรก็ตาม Donut Lab ไม่ได้ระบุวัสดุเฉพาะที่จำเป็นในการผลิตเซลล์แบตเตอรี่โซลิดสเตททั้งหมดของตน
แอนทวน กู๊ดวิน นักข่าวอาวุโสในวงการยานยนต์ ได้มีโอกาสสัมผัสกับแบตเตอรี่โซลิดสเตทรุ่นใหม่ของ Donut Lab อย่างใกล้ชิดในงาน CES ปีนี้ จากการแนะนำของเขา แบตเตอรี่รุ่นนี้มีขนาดใกล้เคียงกับสมาร์ทโฟนหน้าจอใหญ่ (เช่น iPhone 17 Pro Max) และมีน้ำหนักเบามาก แบตเตอรี่น้ำหนักเบาพิเศษนี้จะเหมาะอย่างยิ่งสำหรับการใช้งานในโดรนในอนาคต
ตามแผนของ Donut Lab บริษัทจะสร้างโซลูชันเพื่อรวมแบตเตอรี่เหล่านี้เข้าด้วยกันเป็นหน่วยพลังงานขนาดใหญ่ขึ้น 5 kWh โดยแต่ละหน่วยจะมีขนาดใกล้เคียงกับเครื่องเล่นเกม PS5 ขนาดที่เล็กนี้จะช่วยให้สามารถติดตั้งหน่วยพลังงานดังกล่าวได้ถึงสี่หน่วยในโครงของรถจักรยานยนต์ Verge TS Pro การออกแบบที่ก้าวล้ำนี้ได้รับประโยชน์จากมอเตอร์ไฟฟ้าทรงกลมที่รวมอยู่ในล้อ ซึ่ง Donut Lab ได้ประกาศไปเมื่อปีที่แล้ว เมื่อวันจันทร์ที่ผ่านมา Donut Lab และ Verge Motorcycles ประกาศว่ารถจักรยานยนต์ Verge จะเป็นยานพาหนะที่ผลิตในปริมาณมากเป็นครั้งแรกของโลกที่ติดตั้งแบตเตอรี่ใหม่นี้ รถจักรยานยนต์รุ่นนี้ใช้เวลาในการชาร์จเพียง 10 นาที และสามารถวิ่งได้ไกลถึง 60 กิโลเมตรต่อนาที ส่วนรุ่น Verge Ultra สามารถวิ่งได้ไกลถึง 600 กิโลเมตรต่อการชาร์จหนึ่งครั้ง แบตเตอรี่นี้มีอายุการใช้งาน 100,000 รอบการชาร์จ ซึ่งเทียบเท่ากับระยะทางรวมทางทฤษฎี 60 ล้านกิโลเมตร แม้จะขับขี่เพียง 60,000 กิโลเมตรต่อปี แบตเตอรี่นี้ก็สามารถใช้งานได้นานถึง 1,000 ปี หลายคนอาจมองว่า “เป็นเรื่องที่เหลือเชื่อเกินไป”
เมื่อวันจันทร์ที่ผ่านมา Donut Lab และ Verge Motorcycles ประกาศว่ารถจักรยานยนต์ Verge จะเป็นยานพาหนะที่ผลิตในปริมาณมากเป็นครั้งแรกของโลกที่ติดตั้งแบตเตอรี่ใหม่นี้ รถจักรยานยนต์รุ่นนี้ใช้เวลาในการชาร์จเพียง 10 นาที และสามารถวิ่งได้ไกลถึง 60 กิโลเมตรต่อนาที ส่วนรุ่น Verge Ultra สามารถวิ่งได้ไกลถึง 600 กิโลเมตรต่อการชาร์จหนึ่งครั้ง แบตเตอรี่นี้มีอายุการใช้งาน 100,000 รอบการชาร์จ ซึ่งเทียบเท่ากับระยะทางรวมทางทฤษฎี 60 ล้านกิโลเมตร แม้จะขับขี่เพียง 60,000 กิโลเมตรต่อปี แบตเตอรี่นี้ก็สามารถใช้งานได้นานถึง 1,000 ปี หลายคนอาจมองว่า “เป็นเรื่องที่เหลือเชื่อเกินไป”
“Donut Lab ได้คิดค้นแบตเตอรี่แบบโซลิดสเตทประสิทธิภาพสูงรุ่นใหม่ ที่สามารถผลิตได้ในปริมาณมาก และได้เห็นการใช้งานจริงแล้วในรถจักรยานยนต์ Verge Motorcycles ในไตรมาสที่ 1 ปี 2026” ราคาเริ่มต้นของ Verge TS Pro อยู่ที่ 29,900 ดอลลาร์สหรัฐ  นอกจากจะนำไปใช้ในรถจักรยานยนต์ไฟฟ้าแล้ว แบตเตอรี่โซลิดสเตทก็ดูมีอนาคตที่สดใสกว่ามากในการนำไปใช้กับรถยนต์ไฟฟ้า กู๊ดวินกล่าวว่าข้อดีของเทคโนโลยีนี้จะเห็นได้ชัดเจนยิ่งขึ้นในรถยนต์ขนาดใหญ่ การลดน้ำหนักและความเร็วในการชาร์จที่เพิ่มขึ้นจะส่งผลให้การใช้งานมีประสิทธิภาพมากขึ้นเป็นสองเท่า เมื่อวันจันทร์ที่ผ่านมา โดนัทแล็บได้ประกาศว่าจะร่วมมือกับบริษัทรถยนต์ไฟฟ้า WattEV เพื่อสร้างแพลตฟอร์มรถยนต์ไฟฟ้าแบบโมดูลาร์น้ำหนักเบาพิเศษที่ผสมผสานเทคโนโลยีมอเตอร์และแบตเตอรี่ของโดนัทเข้าด้วยกัน
นอกจากจะนำไปใช้ในรถจักรยานยนต์ไฟฟ้าแล้ว แบตเตอรี่โซลิดสเตทก็ดูมีอนาคตที่สดใสกว่ามากในการนำไปใช้กับรถยนต์ไฟฟ้า กู๊ดวินกล่าวว่าข้อดีของเทคโนโลยีนี้จะเห็นได้ชัดเจนยิ่งขึ้นในรถยนต์ขนาดใหญ่ การลดน้ำหนักและความเร็วในการชาร์จที่เพิ่มขึ้นจะส่งผลให้การใช้งานมีประสิทธิภาพมากขึ้นเป็นสองเท่า เมื่อวันจันทร์ที่ผ่านมา โดนัทแล็บได้ประกาศว่าจะร่วมมือกับบริษัทรถยนต์ไฟฟ้า WattEV เพื่อสร้างแพลตฟอร์มรถยนต์ไฟฟ้าแบบโมดูลาร์น้ำหนักเบาพิเศษที่ผสมผสานเทคโนโลยีมอเตอร์และแบตเตอรี่ของโดนัทเข้าด้วยกัน
มาร์โก เลห์ติแมกิ ประธานเจ้าหน้าที่บริหารของโดนัทแล็บ กล่าวว่า "แบตเตอรี่โซลิดสเตทมักถูกกล่าวว่า 'อีกไม่กี่ปีข้างหน้าก็จะพร้อมใช้งาน' แต่คำตอบของเราแตกต่างออกไป แบตเตอรี่เหล่านี้พร้อมใช้งานแล้วในวันนี้ ไม่ใช่ในอนาคต"
เพื่อให้เข้าใจได้ดียิ่งขึ้น ลองมาดูแบตเตอรี่ที่ใช้ในเชิงพาณิชย์ในปัจจุบันกัน ในอุตสาหกรรมแบตเตอรี่นั้นมี "ไตรลักษณ์ที่เป็นไปไม่ได้" (Mundellian Trilemma) หรือ "สามสิ่งที่เป็นไปไม่ได้" มาโดยตลอด ซึ่งหมายถึงความยากลำบากในการสร้างสมดุลระหว่างตัวชี้วัดหลักสามประการของแบตเตอรี่ (ประสิทธิภาพ ต้นทุน และความปลอดภัย) การเพิ่มประสิทธิภาพในด้านใดด้านหนึ่งมักต้องแลกมาด้วยการเสียสละอีกด้านหนึ่ง หรืออาจถึงสองด้านด้วยซ้ำ
เมื่อเปรียบเทียบกันแล้ว แบตเตอรี่ลิเธียมไอออนเชิงพาณิชย์ชั้นนำมีความหนาแน่นพลังงานประมาณ 250 ถึง 300 Wh/kg โดยมีอายุการใช้งานโดยทั่วไปประมาณ 5000 รอบการชาร์จ เพื่อยืดอายุการใช้งานแบตเตอรี่ มักไม่แนะนำให้ชาร์จเกิน 80% หากคุณสมบัติทั้งหมดของแบตเตอรี่โดนัทเป็นจริง มันก็เหนือกว่าเทคโนโลยีที่มีอยู่เดิมในทุกด้านอย่างแท้จริง
ผู้ผลิตแบตเตอรี่รายอื่น ๆ มีความคืบหน้าอย่างไรบ้าง? พวกเขามีแผนอย่างไรสำหรับการผลิตแบตเตอรี่โซลิดสเตทแบบโพลีเมอร์ (ASSB) ในปริมาณมาก? ซันโวด้าประกาศเมื่อเดือนตุลาคม 2025 เกี่ยวกับแบตเตอรี่โซลิดสเตทแบบโพลีเมอร์รุ่นใหม่ที่มีความหนาแน่นพลังงาน 400 Wh/kg ซึ่งมีอายุการใช้งานเพียง 1200 รอบการชาร์จ แบตเตอรี่ซูเปอร์เชนซิงรุ่นที่สองที่ CATL เปิดตัวในเดือนเมษายน 2025 ก็ได้วางจำหน่ายแล้วเช่นกัน โดยมีระยะทางการวิ่ง 520 กิโลเมตรต่อการชาร์จ 5 นาที ส่วนแบตเตอรี่ LFP รุ่นที่ห้ามีอายุการใช้งานประมาณ 3000 รอบการชาร์จขึ้นไป
เดิมทีโตโยต้ามีแผนจะเริ่มการผลิตแบตเตอรี่โซลิดสเตทจำนวนมากในปี 2020 แต่ต่อมาได้เลื่อนออกไปเป็นปี 2023 จากนั้นเป็นปี 2026 และปัจจุบันกำหนดไว้ที่ปี 2027-2028 ส่วนซัมซุง เอสดีไอ ก็ตั้งเป้าหมายที่จะผลิตแบตเตอรี่โซลิดสเตทในปริมาณมากได้ในปี 2027 เช่นกัน
CATL มีแผนว่าจะเริ่มการผลิตแบตเตอรี่โซลิดสเตทขนาดเล็กในปี 2027 และการผลิตขนาดใหญ่ประมาณปี 2030 ส่วน Hyundai และ Kia กล่าวว่าจะไม่เร็วกว่าปี 2030 Bloomberg NEF คาดการณ์ว่าแม้กระทั่งในปี 2035 แบตเตอรี่โซลิดสเตททั้งหมดก็จะมีส่วนแบ่งการตลาดทั่วโลกจากรถยนต์ไฟฟ้าและระบบจัดเก็บพลังงานเพียงประมาณ 10% เท่านั้น

 ในงาน CES 2026 Donut Lab ได้ประกาศเปิดตัวสิ่งที่พวกเขาเรียกว่าแบตเตอรี่โซลิดสเตทแบบเต็มรูปแบบรุ่นแรกของโลก ซึ่งพร้อมสำหรับการผลิตในระดับ OEM และจะเป็นแบตเตอรี่ชนิดแรกที่จะนำไปใช้กับรถจักรยานยนต์รุ่น TS Pro และ Ultra ของ Verge Motorcycles หากสามารถส่งมอบให้กับลูกค้าได้จริง นี่จะเป็นก้าวสำคัญในเส้นทางการใช้พลังงานไฟฟ้าทั่วโลก โดยเป็นการบ่งชี้ถึงการเปลี่ยนผ่านของเทคโนโลยีโซลิดสเตทจากห้องปฏิบัติการไปสู่การผลิตจำนวนมาก
ในงาน CES 2026 Donut Lab ได้ประกาศเปิดตัวสิ่งที่พวกเขาเรียกว่าแบตเตอรี่โซลิดสเตทแบบเต็มรูปแบบรุ่นแรกของโลก ซึ่งพร้อมสำหรับการผลิตในระดับ OEM และจะเป็นแบตเตอรี่ชนิดแรกที่จะนำไปใช้กับรถจักรยานยนต์รุ่น TS Pro และ Ultra ของ Verge Motorcycles หากสามารถส่งมอบให้กับลูกค้าได้จริง นี่จะเป็นก้าวสำคัญในเส้นทางการใช้พลังงานไฟฟ้าทั่วโลก โดยเป็นการบ่งชี้ถึงการเปลี่ยนผ่านของเทคโนโลยีโซลิดสเตทจากห้องปฏิบัติการไปสู่การผลิตจำนวนมาก ในข่าวประชาสัมพันธ์บนเว็บไซต์อย่างเป็นทางการ Donut Lab ระบุว่า บริษัทมุ่งมั่นที่จะคิดค้นและนำเสนอโซลูชันด้านการใช้พลังงานไฟฟ้าแบบใหม่ๆ โดยผลักดันขีดจำกัดด้านประสิทธิภาพของยานยนต์ไฟฟ้าอย่างไม่หยุดยั้ง และนำเทคโนโลยีใหม่ๆ สู่ตลาด Donut Lab กำลังกำหนดอนาคตของการคมนาคมขนส่ง “ขณะนี้ Donut Lab รู้สึกเป็นเกียรติอย่างยิ่งที่ได้เปิดตัวแบตเตอรี่โซลิดสเตทตัวแรกของโลกที่สามารถนำไปใช้ในการผลิตยานยนต์ OEM ได้ แบตเตอรี่โซลิดสเตทของ Donut Lab จะถูกนำไปใช้งานเชิงพาณิชย์ทันที เพื่อให้พลังงานแก่รถจักรยานยนต์ Verge รุ่นปัจจุบัน”
ในข่าวประชาสัมพันธ์บนเว็บไซต์อย่างเป็นทางการ Donut Lab ระบุว่า บริษัทมุ่งมั่นที่จะคิดค้นและนำเสนอโซลูชันด้านการใช้พลังงานไฟฟ้าแบบใหม่ๆ โดยผลักดันขีดจำกัดด้านประสิทธิภาพของยานยนต์ไฟฟ้าอย่างไม่หยุดยั้ง และนำเทคโนโลยีใหม่ๆ สู่ตลาด Donut Lab กำลังกำหนดอนาคตของการคมนาคมขนส่ง “ขณะนี้ Donut Lab รู้สึกเป็นเกียรติอย่างยิ่งที่ได้เปิดตัวแบตเตอรี่โซลิดสเตทตัวแรกของโลกที่สามารถนำไปใช้ในการผลิตยานยนต์ OEM ได้ แบตเตอรี่โซลิดสเตทของ Donut Lab จะถูกนำไปใช้งานเชิงพาณิชย์ทันที เพื่อให้พลังงานแก่รถจักรยานยนต์ Verge รุ่นปัจจุบัน” Donut Lab ระบุว่าประสิทธิภาพของแบตเตอรี่ได้รับการทดสอบอย่างเข้มงวดในอุณหภูมิที่ตั้งแต่ -30 ถึงมากกว่า 100 องศาเซลเซียส (โดยยังคงรักษาความจุได้ 99 เปอร์เซ็นต์ “โดยไม่มีสัญญาณของการติดไฟหรือการเสื่อมสภาพ”)
Donut Lab ระบุว่าประสิทธิภาพของแบตเตอรี่ได้รับการทดสอบอย่างเข้มงวดในอุณหภูมิที่ตั้งแต่ -30 ถึงมากกว่า 100 องศาเซลเซียส (โดยยังคงรักษาความจุได้ 99 เปอร์เซ็นต์ “โดยไม่มีสัญญาณของการติดไฟหรือการเสื่อมสภาพ”) เมื่อวันจันทร์ที่ผ่านมา Donut Lab และ Verge Motorcycles ประกาศว่ารถจักรยานยนต์ Verge จะเป็นยานพาหนะที่ผลิตในปริมาณมากเป็นครั้งแรกของโลกที่ติดตั้งแบตเตอรี่ใหม่นี้ รถจักรยานยนต์รุ่นนี้ใช้เวลาในการชาร์จเพียง 10 นาที และสามารถวิ่งได้ไกลถึง 60 กิโลเมตรต่อนาที ส่วนรุ่น Verge Ultra สามารถวิ่งได้ไกลถึง 600 กิโลเมตรต่อการชาร์จหนึ่งครั้ง แบตเตอรี่นี้มีอายุการใช้งาน 100,000 รอบการชาร์จ ซึ่งเทียบเท่ากับระยะทางรวมทางทฤษฎี 60 ล้านกิโลเมตร แม้จะขับขี่เพียง 60,000 กิโลเมตรต่อปี แบตเตอรี่นี้ก็สามารถใช้งานได้นานถึง 1,000 ปี หลายคนอาจมองว่า “เป็นเรื่องที่เหลือเชื่อเกินไป”
เมื่อวันจันทร์ที่ผ่านมา Donut Lab และ Verge Motorcycles ประกาศว่ารถจักรยานยนต์ Verge จะเป็นยานพาหนะที่ผลิตในปริมาณมากเป็นครั้งแรกของโลกที่ติดตั้งแบตเตอรี่ใหม่นี้ รถจักรยานยนต์รุ่นนี้ใช้เวลาในการชาร์จเพียง 10 นาที และสามารถวิ่งได้ไกลถึง 60 กิโลเมตรต่อนาที ส่วนรุ่น Verge Ultra สามารถวิ่งได้ไกลถึง 600 กิโลเมตรต่อการชาร์จหนึ่งครั้ง แบตเตอรี่นี้มีอายุการใช้งาน 100,000 รอบการชาร์จ ซึ่งเทียบเท่ากับระยะทางรวมทางทฤษฎี 60 ล้านกิโลเมตร แม้จะขับขี่เพียง 60,000 กิโลเมตรต่อปี แบตเตอรี่นี้ก็สามารถใช้งานได้นานถึง 1,000 ปี หลายคนอาจมองว่า “เป็นเรื่องที่เหลือเชื่อเกินไป” นอกจากจะนำไปใช้ในรถจักรยานยนต์ไฟฟ้าแล้ว แบตเตอรี่โซลิดสเตทก็ดูมีอนาคตที่สดใสกว่ามากในการนำไปใช้กับรถยนต์ไฟฟ้า กู๊ดวินกล่าวว่าข้อดีของเทคโนโลยีนี้จะเห็นได้ชัดเจนยิ่งขึ้นในรถยนต์ขนาดใหญ่ การลดน้ำหนักและความเร็วในการชาร์จที่เพิ่มขึ้นจะส่งผลให้การใช้งานมีประสิทธิภาพมากขึ้นเป็นสองเท่า เมื่อวันจันทร์ที่ผ่านมา โดนัทแล็บได้ประกาศว่าจะร่วมมือกับบริษัทรถยนต์ไฟฟ้า WattEV เพื่อสร้างแพลตฟอร์มรถยนต์ไฟฟ้าแบบโมดูลาร์น้ำหนักเบาพิเศษที่ผสมผสานเทคโนโลยีมอเตอร์และแบตเตอรี่ของโดนัทเข้าด้วยกัน
นอกจากจะนำไปใช้ในรถจักรยานยนต์ไฟฟ้าแล้ว แบตเตอรี่โซลิดสเตทก็ดูมีอนาคตที่สดใสกว่ามากในการนำไปใช้กับรถยนต์ไฟฟ้า กู๊ดวินกล่าวว่าข้อดีของเทคโนโลยีนี้จะเห็นได้ชัดเจนยิ่งขึ้นในรถยนต์ขนาดใหญ่ การลดน้ำหนักและความเร็วในการชาร์จที่เพิ่มขึ้นจะส่งผลให้การใช้งานมีประสิทธิภาพมากขึ้นเป็นสองเท่า เมื่อวันจันทร์ที่ผ่านมา โดนัทแล็บได้ประกาศว่าจะร่วมมือกับบริษัทรถยนต์ไฟฟ้า WattEV เพื่อสร้างแพลตฟอร์มรถยนต์ไฟฟ้าแบบโมดูลาร์น้ำหนักเบาพิเศษที่ผสมผสานเทคโนโลยีมอเตอร์และแบตเตอรี่ของโดนัทเข้าด้วยกัน



