Что такое гидроксид лития и где мы его используем?
| Jerry Huang
Гидроксид лития — сильное основание, и его химические свойства больше похожи на свойства гидроксидов элементов 2-й группы периодической таблицы, чем на свойства гидроксидов элементов 1-й группы. Гидроксид лития, химическая формула LiOH, молекулярная масса 23,95, белый тетрагональный кристалл, обладает сильной коррозионной активностью и раздражает кожу человека, температура плавления 450℃ (842℉), относительная плотность 1,46. Температура дифференцирования составляет 924℃ (1695℉). Он слабо растворим в этаноле, растворим в воде, но его растворимость ниже, чем у гидроксидов других щелочных металлов.
После поглощения влаги из воздуха или кристаллизации в водном растворе получают моногидрат гидроксида лития. Гидроксид лития реагирует с кислыми газами, такими как диоксид серы, хлористый водород, цианистый водород и др. Он также может полностью реагировать с сильными или слабыми кислотами в водных растворах. Он поглощает углекислый газ из воздуха, образуя карбонат лития. Гидроксид лития используется в качестве добавки к смазочным материалам (загуститель, антиоксидант, противозадирный агент), которая может улучшить термостойкость, водостойкость, стабильность и механические свойства; а литиевые смазки часто используются для подшипников в автомобилях, поездах, самолетах, кранах и любых ценных машинах.
Литийгидроксид аккумуляторного класса с низкой температурой плавления широко используется в качестве лучшего электролитного материала в производстве литий-ионных батарей на основе никельсодержащих соединений (NCA и NCM), что обеспечивает литий-ионным батареям с высоким содержанием никеля гораздо лучшие электрические свойства, чем карбонат лития; при этом последний до сих пор остается приоритетным выбором для литий-железо-фосфатных (LFP) и многих других типов батарей.
Обожженный твердый гидроксид лития может использоваться в качестве поглотителя углекислого газа для экипажей космических аппаратов и подводных лодок. Углекислый газ легко поглощается газом, содержащим водяной пар. Формула химической реакции выглядит следующим образом: 2LiOH + CO2 → Li2CO3 + H2O
Один грамм безводного гидроксида лития способен поглотить 450 мл углекислого газа, а 750 г достаточно, чтобы поглотить весь выдыхаемый человеком углекислый газ за сутки. Кроме того, гидроксид лития в основном используется для производства различных соединений лития и солей лития, а также литиевых мыл, литиевых смазок и алкидных смол. Он также широко используется в качестве катализаторов, фотопроявителей, проявителей для спектрального анализа, добавок в щелочные батареи. В качестве добавки к электролиту щелочных батарей гидроксид лития может увеличить электрическую емкость на 12–15% и срок службы батареи в 2–3 раза.
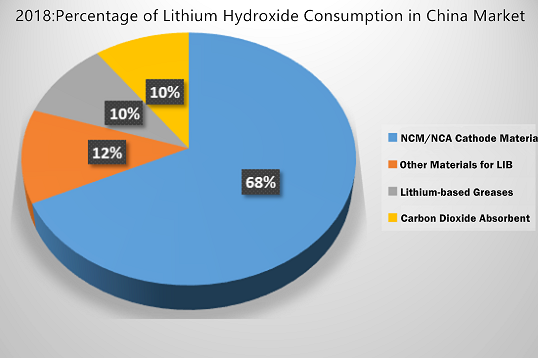
Для вашего означения, вот данные о потреблении гидроксида лития на китайском рынке в 2018 году.