Является ли LiTFSI наилучшим выбором для улучшения характеристик HEV при низких температурах?
| Jerry Huang
В целом считается, что чем выше доля твердого углерода (более 15%), нанесенного на анод литий-ионного аккумулятора, тем лучше его проводимость. Однако следует уточнить, что плотность покрытия из чистого твердого углерода составляет около 1,15 г/см³. Если на графитовый материал нанесено больше твердого углерода, плотность покрытия всего полюсного наконечника снизится (без увеличения пространства между слоями основного материала). В лучшем случае она составит 1,2 г/см³. При этом твердый углерод может уплотниться, и его характеристики могут быть использованы не в полной мере. Поэтому необходимо выбирать различное соотношение твердого углерода в зависимости от сценария применения.
Здравый смысл подсказывает, что анодный материал обычно имеет неравномерное распределение напряжений и неправильную форму. Чем больше размер частиц материала, тем выше внутреннее сопротивление. Поэтому, если используется твердое углеродное покрытие, хотя срок службы батареи может быть значительно увеличен, ее календарный срок службы относительно невелик (емкость элемента батареи значительно снижается в течение 6 месяцев хранения).
Является ли LiTFSI наилучшим выбором для улучшения характеристик HEV при низких температурах?
Очевидно, что твердого анодного материала с углеродным покрытием недостаточно для решения проблемы низкой производительности при низких температурах; необходимо улучшить другие материалы, такие как электролиты. Электролиты являются важной частью литий-ионных батарей, и они не только определяют скорость миграции ионов лития Li+ в жидкой фазе, но и играют ключевую роль в формировании пленки SEI. В то же время существующие электролиты имеют более низкую диэлектрическую постоянную, поэтому ионы лития могут притягивать больше молекул растворителя и высвобождать их во время десольвации, вызывая большие изменения энтропии системы и более высокие температурные коэффициенты (ТК). Поэтому важно найти метод модификации, который имеет меньшее изменение энтропии во время десольвации, более низкий температурный коэффициент и меньше зависит от концентрации электролита. В настоящее время существует два способа улучшения низкотемпературных характеристик с помощью электролитов:
- Улучшение низкотемпературной проводимости электролитов достигается за счет оптимизации состава растворителя. Низкотемпературные характеристики электролитов определяются низкотемпературной эвтектической точкой. Если температура плавления слишком высока, электролит может кристаллизоваться при низких температурах, что серьезно повлияет на проводимость электролитов и в конечном итоге приведет к выходу из строя литиевой батареи. этиленкарбонат (ЭК) является важным компонентом растворителя электролита. Его температура плавления составляет 36 °C. При низких температурах его растворимость может снижаться, и даже происходит осаждение кристаллов в электролитах. Добавление низкоплавких и низковязких компонентов для разбавления и снижения содержания ЭК в растворителе позволяет эффективно снизить вязкость и эвтектическую точку электролита при низких температурах, а также улучшить его проводимость. Кроме того, исследования, проведенные как в стране, так и за рубежом, показали, что использование цепных карбоновых кислот, этилацетата, этилпропионата, метилацетата и метилбутирата в качестве сорастворителя электролита способствует улучшению низкотемпературной проводимости электролитов и значительно повышает низкотемпературные характеристики батареи. В этой области достигнут значительный прогресс.
- Использование новых добавок для улучшения свойств SEI-пленки способствует проводимости ионов лития при низких температурах. Электролитная соль является одним из важных компонентов электролитов, а также ключевым фактором для достижения превосходных характеристик при низких температурах. С 2021 года в качестве электролитной соли широко используется гексафторфосфат лития. SEI-пленка, легко образующаяся после старения, имеет высокое сопротивление, что приводит к плохим характеристикам при низких температурах. Поэтому разработка нового типа литиевой соли становится актуальной задачей. Тетрафторборат лития и дифтороксалат лития (LiODFB), как литиевые соли для электролита, также обеспечивают высокую проводимость при высоких и низких температурах, благодаря чему литий-ионные батареи демонстрируют превосходные электрохимические характеристики в широком диапазоне температур.
LiTFSI, как новый тип неводной литиевой соли, обладает высокой термической стабильностью, низкой степенью ассоциации анионов и катионов, а также высокой растворимостью и диссоциацией в карбонатных системах. При низких температурах высокая проводимость и низкое сопротивление переносу заряда электролита системы LiFSI обеспечивают его работу при низких температурах. Мандал и др. использовали LiTFSI в качестве литиевой соли и EC/DMC/EMC/pC (массовое соотношение 15:37:38:10) в качестве основного растворителя для электролита; и результаты показали, что электролит сохраняет высокую проводимость 2 мСм·см⁻¹ при -40 °C. Поэтому LiTFSI считается наиболее перспективным электролитом, способным заменить гексафторфосфат лития, а также рассматривается как альтернатива для перехода к эре твердых электролитов.
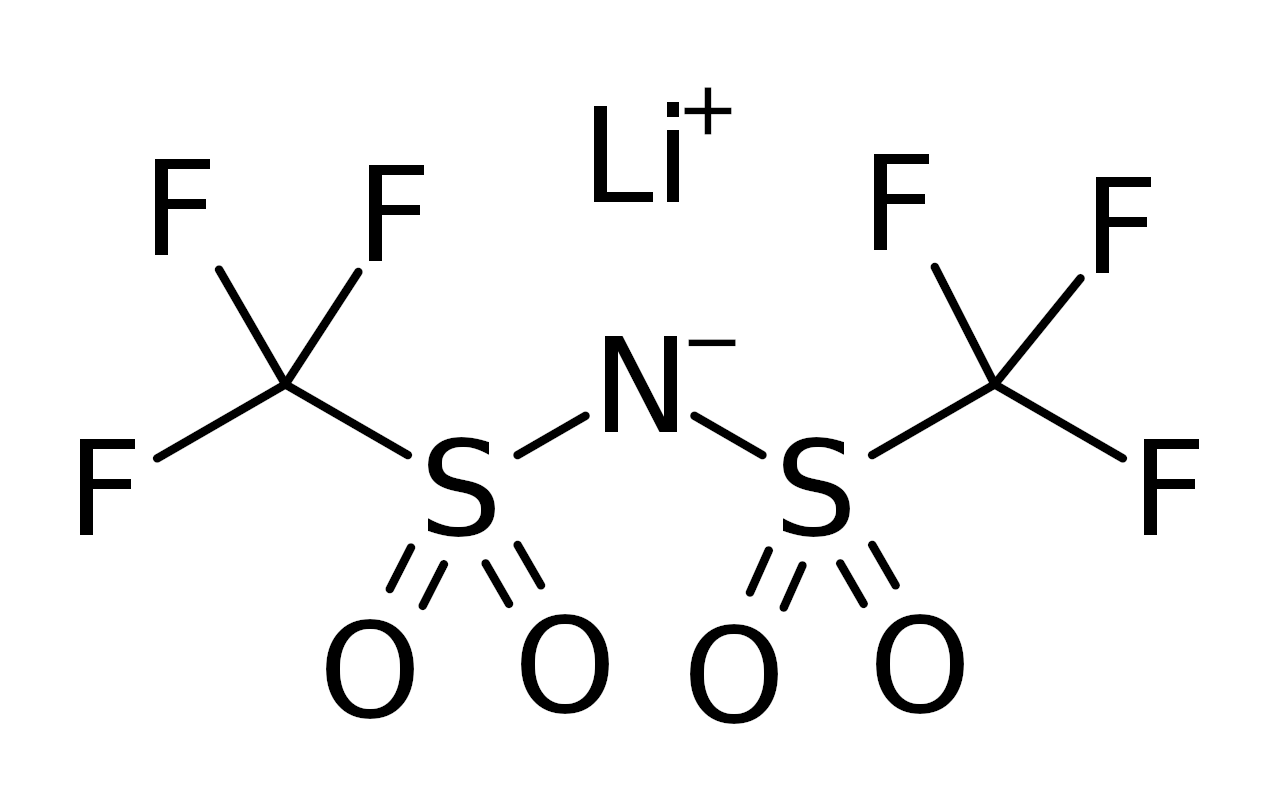
Согласно Википедии, бис(трифторметансульфонил)имид лития, часто обозначаемый просто как LiTFSI, представляет собой гидрофильную соль с химической формулой LiC2F6NO4S2. LiTFSI — это белый кристалл или порошок, который может использоваться в качестве органического электролита на основе литиевой соли для литий-ионных батарей, что обеспечивает высокую электрохимическую стабильность и проводимость электролита. Он широко используется в качестве источника ионов лития в электролитах для литий-ионных батарей как более безопасная альтернатива широко используемому гексафторфосфату лития. Он состоит из одного катиона лития и аниона бистрифлимида. Благодаря очень высокой растворимости в воде (> 21 м), LiTFSI используется в качестве литиевой соли в водно-солевых электролитах для водных литий-ионных батарей.
LiTFSI можно получить реакцией бис(трифторметилсульфонил)имида с гидроксидом лития или карбонатом лития в водном растворе, а безводный вариант — вакуумной сушкой при 110 °C: LiOH + HNTf2 → LiNTf2 + H2O
Бис(трифторметилсульфонил)имид лития может использоваться для приготовления электролитов для литиевых батарей и в качестве нового катализатора Льюиса для редкоземельных элементов; он применяется для получения хиральных имидазолиевых солей путем реакции замещения анионов соответствующих трифторметансульфонатов. Этот продукт является важным фторсодержащим органическим ионным соединением, используемым во вторичных литиевых батареях, суперконденсаторах Chemicalbook, алюминиевых электролитических конденсаторах, высокоэффективных неводных электролитных материалах и в качестве нового высокоэффективного катализатора. Его основные области применения следующие:
- Литиевые батареи
- Ионные жидкости
- Антистатический
- Медицина (гораздо менее распространенное явление)
Однако один инженер-исследователь из Китая однажды сказал: «LiTFSI в основном используется в качестве добавки в современных электролитах и не применяется в качестве основной соли сам по себе. Кроме того, даже если он используется в качестве добавки, разработанный электролит обладает лучшими характеристиками, чем другие электролиты. Электролит на основе LiTFSI намного дороже обычных типов электролитов, поэтому LiTFSI не добавляют, если нет особых требований к характеристикам электролита».
Считается, что в некоторых сценариях применения предъявляются существенные требования к мощным батареям, например, в электрических погрузчиках и автоматизированных транспортных средствах (AGV). Помимо вопросов долговечности и характеристик производственного оборудования, необходимо одновременно решать проблемы срока службы и работы при низких температурах. Поэтому исследования и разработки электролитов следующего поколения будут продолжаться. Однако это по-прежнему многогранная проблема и конкуренция между производительностью, стоимостью и безопасностью; и в конечном итоге рынок сделает свой собственный выбор.
Ссылки:
- Чжэн Хунхэ; Цюй Цюньтин; Чжан Ли; Лю Гао; Батталья Винсент (2012). «Твердый углерод: перспективный анод литий-ионной батареи для высокотемпературных применений с ионным электролитом». RSC Advances. Королевское химическое общество. (11): 4904–4912. doi:10.1039/C2RA20536J. Получено 15.08.2020.
- Камияма, Азуса; Кубота, Кей; Накано, Такеши; Фудзимура, Шун; Шираиши, Соши; Цукада, Хидехико; Комаба, Шиничи (27.01.2020). «Высокоемкостный твердый углерод, синтезированный из макропористой фенольной смолы, для натрий-ионных и калий-ионных батарей». ACS Applied Energy Materials. Американское химическое общество. 3: 135–140. doi:10.1021/acsaem.9b01972.
- Хосрави, Мохсен; Баширпур, Неда; Нематпур, Фатеме (01.11.2013). «Синтез твердого углерода в качестве анодного материала для литий-ионных батарей». Advanced Materials Research. 829: 922–926. doi:10.4028/www.scientific.net/AMR.829.922. S2CID 95359308. Дата обращения: 15.08.2020.
- Горипарти, Субрахманьям; Миле, Эрманно; Де Анджелис, Франческо; Ди Фабрицио, Энцо; Пройетти Заккария, Ремо; Капилья, Клаудио (2014). «Обзор последних достижений в области наноструктурированных анодных материалов для литий-ионных батарей». Журнал источников энергии. 257: 421–443. Бибкод: 2014JPS...257..421G. doi:10.1016/j.jpowsour.2013.11.103.
- Ирисарри, Э.; Понруч, А.; Паласин, М.Р. (2015). «Обзор – Материалы для твердых углеродных отрицательных электродов для натрий-ионных батарей». Журнал Электрохимического общества. 162: A2476. doi:10.1149/2.0091514jes.
- Доу, Синьвэй; Хаса, Ивана; Саурель, Дамьен; Ваалма, Кристоф; Ву, Лиминг; Бухгольц, Даниэль; Брессер, Доминик; Комаба, Шиничи; Пассерини, Стефано (2019). «Твердые углеродные материалы для натрий-ионных батарей: структура, анализ, устойчивость и электрохимия». Materials Today. 23: 87–104. doi:10.1016/j.mattod.2018.12.040